細胞治療
我國免疫細胞治療產業發展概況(一)
免疫細胞治療是指將體外活化和擴增的自體或異體免疫效應細胞輸注患者體內的治療方法。自2017年FDA批準全球首個CAR-T藥物-諾華的Kymriah上市以來,免疫細胞細胞研發熱度就一直居高不下,目前全球獲批上市的CAR-T產品共有3款分別是諾華的Kymriah、凱特的YESCARTA和Tecartus。我國在免疫細胞治療產品的研發水平僅次于美國,本文將針對目前國內獲得CDE受理的免疫細胞治療產品進行分析。
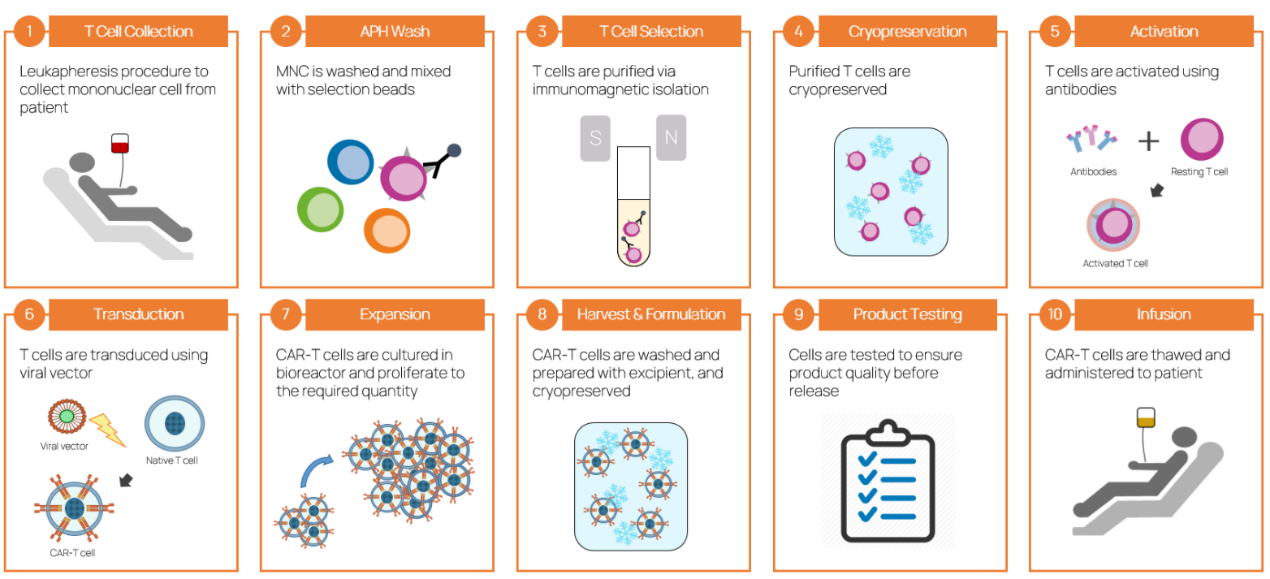
圖:CAR-T細胞產品治療過程
數據來源:根據公開資料整理
全國共有40個產品獲得CDE受理,上海遙遙領先
目前我國共有35家企業的40個產品獲得CDE受理,上海無論是產品數量還是企業數量均遙遙領先處于第一梯隊,深圳、蘇州、北京處于第二梯隊,武漢、南京、重慶、天津、石家莊、廣州、成都則處于第三梯隊。
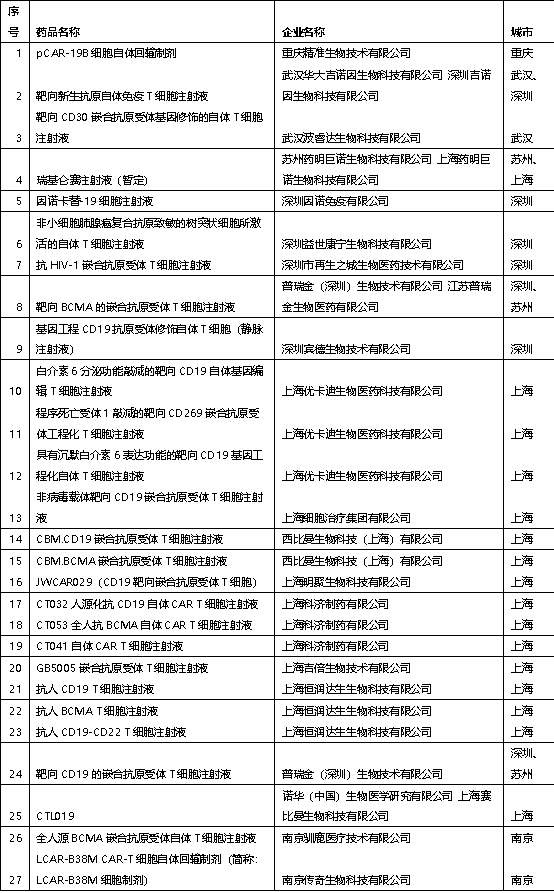
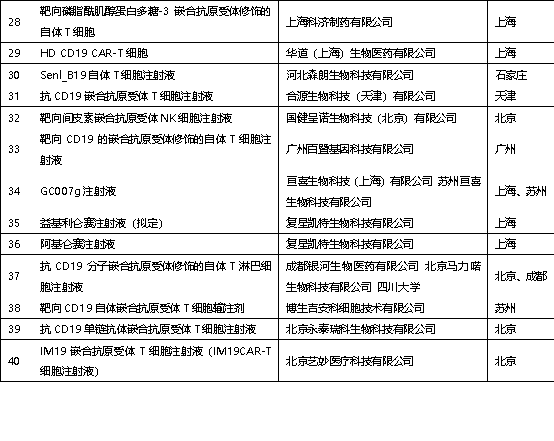
圖:國內獲得CDE受理的免疫細胞治療產品
數據來源:CDE
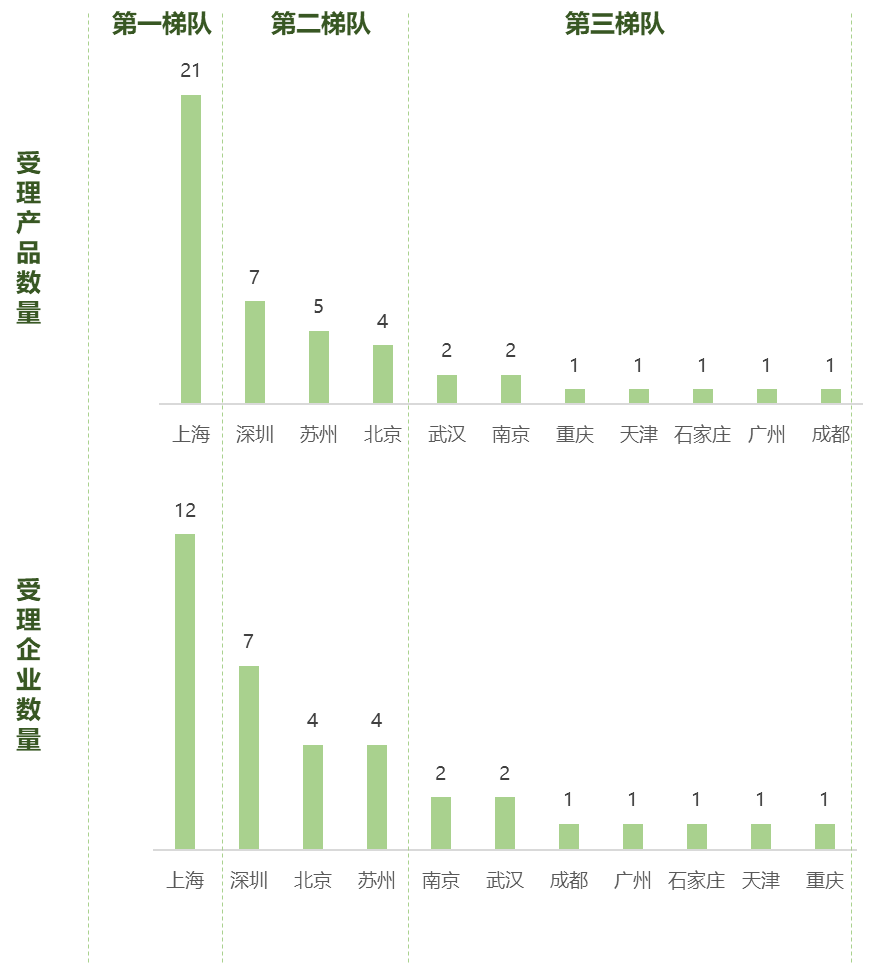
圖:各城市獲得CDE受理的免疫細胞治療產品和企業數量對比
數據來源:CDE
第一梯隊——上海免疫細胞治療產業發展概況
上海獲得CDE受理的免疫細胞產品數量占比超過全國一半,企業數量超過全國的三分之一,這與上海政府高度重視這一產業的發展密切相關。
上海張江地區是我國乃至全球最有潛力發展細胞治療產業的地區之一,目前在該領域已形成先發優勢。據不完全統計,目前圍繞整個細胞治療上下游產業鏈的企業在張江科學城超過50家。其中,細胞治療研發企業超過20家,試劑、設備、耗材、細胞培養基等細胞裝備企業超過15家,相關細胞應用評估、基因檢測企業超過15家。
2019年上海市科委已正式批復同意成立上海張江細胞產業園。根據規劃,張江細胞產業園將以“醫谷”40萬平方米空間為起點,在2019年-2022年初步形成細胞全產業鏈;在2023年-2026年形成從存儲、研發、生產、運輸、治療到裝備為一體的完整成熟的細胞全產業鏈;在2027年-2030年使細胞全產業鏈具有全球影響力。
目前上海聚集了諾華(中國)生物醫學研究有限公司、復星凱特、藥明巨諾、西比曼、優卡迪、亙喜生物等一大批優質企業。
復星凱特
復星凱特生物科技有限公司為復星醫藥集團與美國Kite Pharma(吉利德旗下公司)的合營企業,復星凱特2017年初從美國Kite Pharma引進Yescarta,獲得全部技術授權,并擁有其在中國包括香港、澳門的商業化權利,該產品將被開發用于治療兩線或以上系統性治療后復發或難治性大B細胞淋巴瘤,包括:彌漫性大B細胞淋巴瘤(DLBCL)非特指型、原發性縱隔B細胞淋巴瘤(PMBCL)、高級別B細胞淋巴瘤和濾泡淋巴瘤轉化的DLBCL。
除Yescarta以外,復星凱特同時在上述地區享有Kite Pharma后續產品授權許可的優先選擇權。公司2000平米的細胞治療研發中心于2019年初落成,研發管線還包括多個 CAR-T/TCR-T 臨床階段品種和早期創新研發項目;并且與國內外腫瘤免疫治療領域優秀研發機構合作,打造可持續的創新研發管線。
目前復星凱特引入引進得益基利侖賽注射液(擬定)(Yescarta)正處于上市前最后得行政審批階段,有望成為我國第一個上市的免疫細胞治療產品。另一款產品阿基侖賽注射液的臨床試驗申請已經在今年三月份獲得CDE受理。
上海藥明巨諾
由藥明生物和巨諾醫療共同成立,目前共有7款在研產品,其中包括三款血液腫瘤產品和四款實體瘤產品,進展最快的瑞基侖賽注射液(暫定)目前已經處于上市申請階段。其在上海的設立的研發中心面積2500平米,建立了包括細胞治療過程開發、載體開發、流式細胞檢測、體外細胞功能檢測、分子檢測在內的綜合細胞治療產品開發平臺,2019年被上海市人民政府認定為"外商投資研發中心"。另外還建有約 4000 平方米符合國際cGMP和QMS標準的生產車間,可以為500名患者生產免疫細胞治療產品。
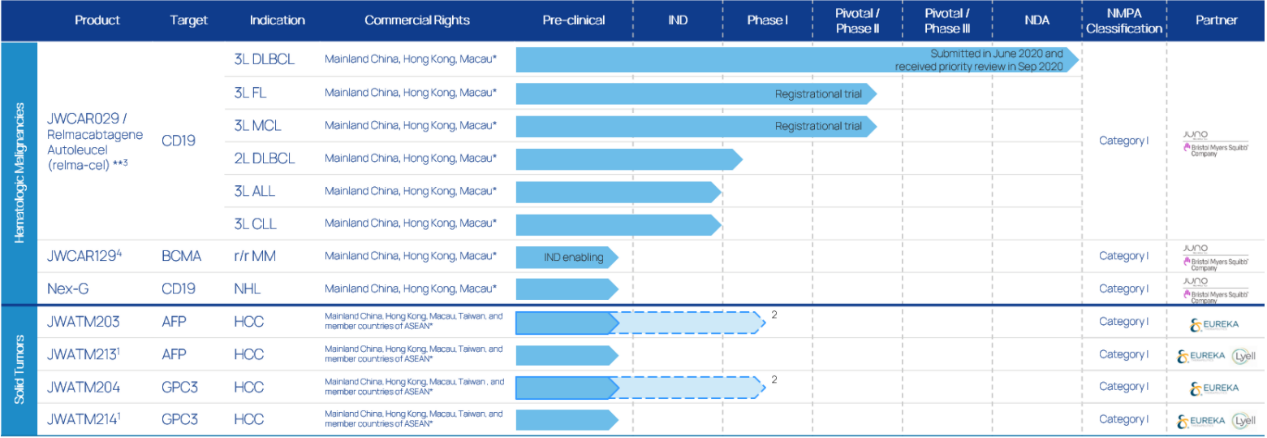
圖:藥明巨諾產品研發管線
數據來源:CDE
優卡迪
優卡迪成立于2015年2月,目前優卡迪不僅完成了從科研-轉化-臨床的技術產品閉合環的建立,而且還打造了CAR-T生產全產業鏈的三個完善的GMP生產和質量管理檢驗體系的生產基地,包括臨床級質粒、慢病毒載體和CAR-T細胞的生產,并且在該生產管理體系下,與國內多家著名大型三甲醫院血液科完成了1000余例CAR-T真實世界的臨床研究和同情性挽救治療,療效達到了和國際臨床試驗中所報道的相一致的預期效果,但在安全性方面凸顯優勢。2019年,歐洲專利局相關人員在Nature Biotechnology發表了CAR-T專利申請和獲批分析,優卡迪排名全球第四。同時優卡迪已獲得了“中國細胞治療企業快速成長獎”、“2019未來醫療100強-中國創新醫藥榜TOP100”、“2020中國醫藥創新企業100強”等多項榮譽,并與海南海藥達成戰略合作,在海南博鰲投資建設基因與細胞治療中心。
目前優卡迪一款沉默白介素6基因的CAR-T產品已經獲批臨床試驗,這款產品具備更低的免疫原性。另一款產品通過沉默PD-1基因,使CAR-T細胞治療效果更好。
西比曼生物
西比曼生物科技集團公司總部坐落于上海張江,擁有6503平方米的細胞GMP生產車間,涵蓋12條獨立的細胞生產線,年產細胞量能夠滿足1萬名癌癥患者和1萬名膝骨關節炎患者的治療需求。公司現有干細胞治療和免疫細胞治療兩個平臺。其中免疫細胞治療平臺主要包含嵌合抗原受體T細胞(CAR-T)、基因工程改造T細胞受體T細胞(TCR-T)以及腫瘤浸潤淋巴細胞(TIL)三類產品。此外公司還在無錫和北京設有細胞產品GMP生產設施。
目前公司有三款免疫細胞治療產品進入臨床試驗,分別為BCMA靶點、CD19/CD20靶點的CAR-T以及一款TCR-T產品。此外公司還與諾華達成戰略合作協議,負責為其在中國生產和供應CAR-T細胞治療藥物Kymriah。
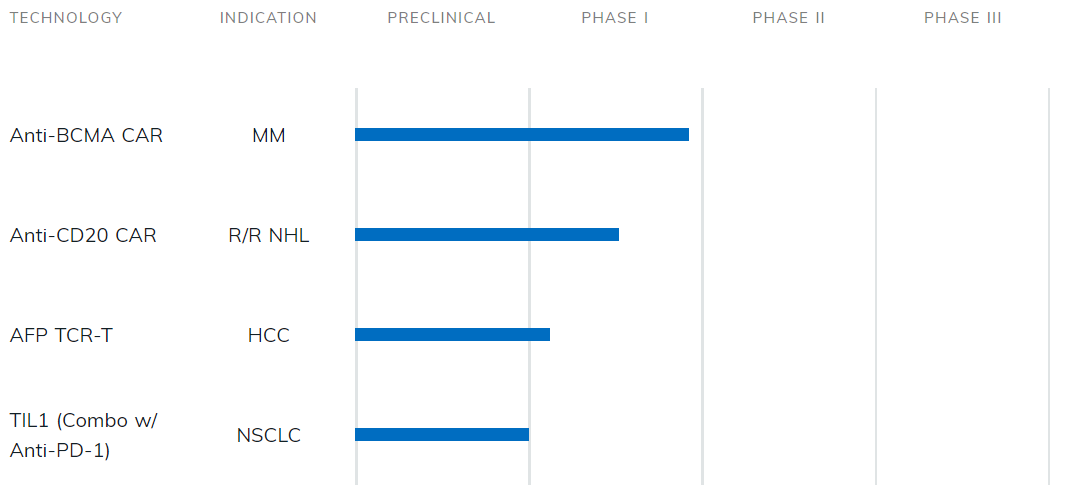
圖:西比曼產品研發管線
數據來源:CDE
科濟生物
科濟生物醫藥(上海)有限公司成立于2014年10月,是中國首家專注于CAR-T細胞免疫治療的創新型企業,也是全球知名的實體腫瘤CAR-T細胞治療研發企業。公司現有員工130多人,碩士及博士學歷員工占65%左右,擁有多名來自輝瑞、羅氏等全球頂尖生物醫藥公司的高管及研發人員。公司擁有包括第四代CAR-T技術在內的八十多項國內外專利技術,自主構建了研發腫瘤靶向抗體的的全人抗體庫與人源化抗體技術平臺,自主研發了能夠覆蓋大部分實體瘤及血液腫瘤的高效特異性CAR-T等候選產品。其中多個項目獲得了新藥創制國家十三五重大專項支持。
目前科濟生物有CT032、CT041、CT053三款產品進入臨床試驗。其中CT041已被NMPA和FDA批準進入臨床試驗,將在北京大學腫瘤醫院、梅奧醫療(Mayo Clinic)等多家國內外著名臨床機構進行開放標簽、多中心、1b期臨床試驗,以評估其治療晚期胃癌、食管胃結合部腺癌或胰腺癌的安全性和有效性。CT053被NMPA授予孤兒藥資格,適應癥為復發難治性多發性骨髓瘤(R/R MM)。

